
Сертификация медицинских изделий считается одним из вариантов оценки соответствия, позволяющим удостовериться, насколько они отвечают существующим нормативным требованиям. Это обусловлено тем, что техника и другие приспособления, предназначенные для медицинских целей, могут причинять вред организму человека косвенным или прямым образом. В подобных ситуациях контроль со стороны уполномоченных надзорных структур играет первоочередную роль.
Специалисты компании «ЕЦЭС КВОЛИТИ» имеют внушительный опыт в сфере подготовки к регистрации и сертификации продукции, предназначенной для оздоровительных целей. Также мы оказываем квалифицированную помощь при сборе документов, необходимых для осуществления испытаний в лабораторных условиях. При отсутствии каких-либо материалов, наши сотрудники готовы заняться их оформлением с соблюдением всех существующих законодательных требований.
или позвоните нам
МСК: +7 499-350-48-69
СПб: +7 812-309-89-10
Сертификация медицинских изделий или получение сертификата соответствия
Речь идет о процедуре проверки изделия, которая выполняется уполномоченными центрами по заявлению изготовителей или лиц, осуществляющих ввоз продукции на территорию РФ. Она позволяет установить, насколько продукт отвечает установленным техническим требованиям, а также документам, в котором представлены общие характеристики объекта стандартизации, или условиям договоров.
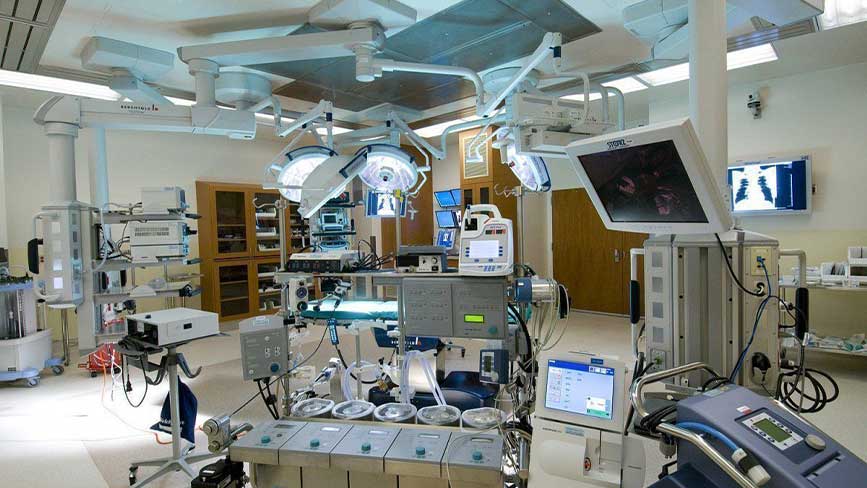
Получение сертификата соответствия на медицинское оборудование в России предполагает выдачу особого документа – Сертификата соответствия, удостоверяющего качество данного товара по его образцу.
Положения к обязательной сертификация продуктов медицинского назначения
Как известно, на лекарственные препараты должна быть получена лицензия, а для ввода в обращение других товаров оздоровительной специфики в РФ и странах-участницах ЕАЭС достаточно получить сертификат соответствия на медицинские изделия.
В список подобных продуктов входят: техника, предметы мебели, аппаратура и другие изделия, применяемые в учреждениях лечебно-профилактического и рекреационного назначения. Они востребованы при выполнении диагностических процедур, лечебных мероприятий, имплантации, лабораторных исследований и других вмешательств, связанных с организмом пациента.
Все вышеуказанные товара классифицируются, в зависимости от степени риска:
- 1 класс (пониженная степень риска): оптические приборы, устройства, используемые для взвешивания людей в медицинских целях;
- 2а класс (средняя степень риска): оборудование, используемое для проведения лабораторных исследований;
- 2б класс (повышенная степень риска): устройства, применяемые для устранения нарушений сердечного ритма, кардиоанализаторы;
- 3 класс (высокая степень риска): внутренние устройства, замещающие функции органов.

Обязательному контролю эффективности и безопасного применения подлежит следующая продукция:
- Имплантаты;
- Техника медицинского назначения;
- Приборы, предназначенные для диагностических и терапевтических процедур;
- Медицинские комплекты;
- Материалы, используемые в хирургических целях;
- Инструменты, предназначенные для медицинского использования;
- Контрольно-измерительные приборы;
- Материалы, используемые в стоматологической практике;
- Протезно-ортопедические приспособления;
- Медизделия из полимеров.
Для изготовителей продукции медицинского назначения, действующих на территории России, может выполняться упрощенная сертификация. Так, при наличии у завода сертификата международного образца ISO 9001, отвечающего стандартам ГОСТ Р ИСО 13485-2004 и ГОСТ Р ИСО 9001-2001, в случае получения получении регистрационного удостоверения и декларации допускается возможность отказа от лабораторных испытаний.
Изделия медицинского назначения и медицинская техника
Чтобы определить, какой вариант оценки соответствия должен использоваться для продуктов оздоровительной специфики, необходимо выяснить, для каких целей они предназначены, и в какой сфере будут применяться. Все вышеуказанные товары подразделяют на изделия медицинского назначения и медицинскую технику.
Мы рассмотрим, какая разрешительная документация требуется на медизделие для его ввода в обращение на рынке:
Изделия медицинского назначения (ИМН). В этом случае речь идет о продуктах, используемых в оздоровительных целях. К их числу относятся различные устройства; средства, предназначенные для проведения перевязок и наложения швов; резиновые и полимерные материалы, применяемые в медицинской практике одновременно или по отдельности для следующих целей:
- В рамках диагностических и лечебных процедур, в профилактических целях, при реализации реабилитационных мероприятий, выполнения медицинских манипуляций и исследований, имплантации, а также восстановления утраченных функциональных способностей, предотвращения беременности;
- Для оказания такого воздействия на организм, которое не предполагает иммунологического, фармакологического, химического или метаболического контакта с ним.
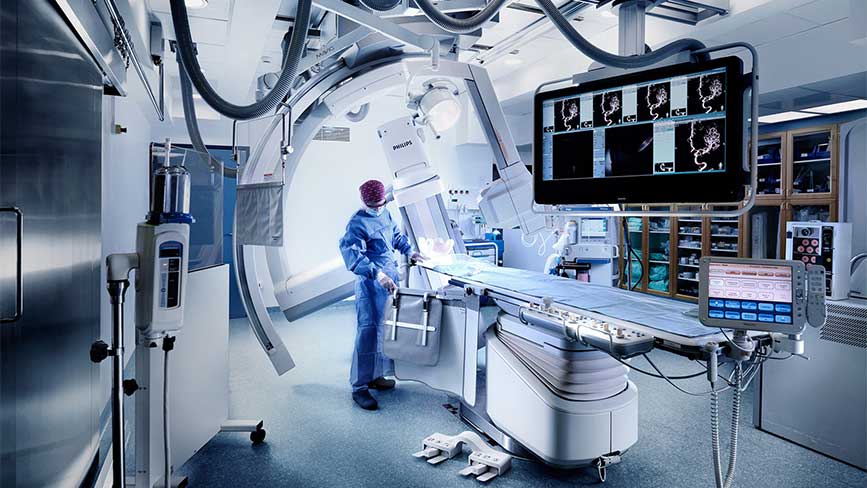
Медицинская техника (ИМТ). В эту группу входят: инструментарий, аппаратура, устройства, приборы, техника, системы с программным обеспечением, которые применяются в следующих целях:
- Для исследовательской деятельности;
- При выполнении диагностических процедур;
- При реализации лечебных мероприятий;
- С целью профилактики;
- Для наблюдения за состоянием организма;
- Для купирования болезненных проявлений;
- С целью компенсации травмы или ограничения двигательной активности;
- Для поддержания жизнедеятельности организма.
То есть, к медицинским изделиям относятся любые устройства, приспособления, инструментарий, аппаратура, материалы и другие продукты, применяемые в комбинации или отдельно, включая компьютерное ПО, позволяющее их использовать в соответствии с предназначением, заявленным изготовителем:
- Для диагностических и профилактических целей, отслеживания состояния организма, реализации лечебных процедур или купирования болезненных симптомов;
- Для выявления, отслеживания, устранения симптомов, лечения или компенсации травмы или ограничения двигательной активности;
- Изучения, имплантации или поддержания жизнедеятельности организма;
- Контроля над зачатием.
или позвоните нам
МСК: +7 499-350-48-69
СПб: +7 812-309-89-10
Порядок выполнения процесса сертификации медицинских изделий
Предоставлять сертификат соответствия на медицинские изделия согласно ГОСТу № 31508-2012 могут уполномоченные центры по сертификации, которые прошли аккредитацию в Федеральном Ведомстве Росстандарта.
Сертификация медизделий выполняется по следующей схеме:
- Изготовитель или импортер продукции предоставляет соответствующее заявление и запрашиваемый пакет документов;
- Производится экспертная оценка предоставленной документации;
- Если в ходе экспертной оценки будет получен положительный результат, изготовитель может рассчитывать на предоставление сертификата соответствия медицинских товаров;
- Происходит оформление и регистрация данного документа;
- Сертификат соответствия на изделия медицинского назначения выдается на руки изготовителю.
Следует отметить, что сертификат соответствия медицинских товаров имеет ограниченный период действия – он предоставляется на 1, 3 или 5 лет. После выдачи документа деятельность изготовителя или импортера на обязательных основаниях должна контролироваться уполномоченной надзорной структурой. Это позволяет убедиться в строгом выполнении требований ГОСТа 31508-2012 в дальнейшем.

ООО «ЕЦЭС КВОЛИТИ» оказывает профессиональную поддержку в сфере подготовки документов, необходимых для выполнения лабораторных испытаний и прохождения сертификации изделий медицинского назначения. Мы имеем дело с медицинской техникой отечественных и иностранных изготовителей. При этом вы можете быть уверены, что весь процесс сертификации медицинских изделий будет осуществляться под контролем грамотных, ответственных и опытных специалистов. При отсутствии необходимых документов, мы готовы заняться их разработкой.
Перечень документов необходимых для получения сертификата соответствия
Далее мы рассмотрим, какие документы необходимо предоставить заявителю в рамках процедуры сертификации:
- ИНН, ОГРН, соглашение на поставку техники медицинского предназначения, Устав и реквизиты предприятия-импортера;
- Название товара медицинского назначения, целевое предназначение, документы эксплуатационного характера, техническая документация;
- Декларация ГОСТ Р. В соответствии с ПП РФ №982 разработка данного документа выполняется в процессе оценки соответствия диагностических масок, инструментария, перчаток, бумажных материалов, средств для перевязки, материалов стоматологического назначения, предметов мебели, катетеров, линз.
- Договор аренды, удостоверяющий право владения производственными цехами.
- РУ (согласно ПП РФ №1416). Информация о ранее выданных разрешительных удостоверениях. Договор о поставке. Для ввозимых товаров — спецификации.
- Заявка на выполнение оценки соответствия, предоставляемая руководителем предприятия-изготовителя или его уполномоченным лицом.
Следует учитывать, что в соответствии с действующим законодательством РФ, декларация соответствия оформляется исключительно на отечественного изготовителя. Если техника оздоровительного назначения импортируется из другой страны, оформление данного документа выполняется на организацию-импортера, который осуществляет свою деятельность на территории РФ.

В ООО «ЕЦЭС КВОЛИТИ» вы будете иметь дело с квалифицированными специалистами, которые обладают внушительным опытом в области сбора информации для целей сертификации, и готовы обеспечить грамотное сопровождение по всем юридическим вопросам. Мы поможем вам в сокращенные сроки получить разрешительные документы, удостоверяющие возможность эффективного и безопасного использования оборудования медицинской специфики, находящегося в обороте. При этом будут четко соблюдены все требования стандартизации и сертификации медицинского товара.
Добровольная сертификация медицинских изделий
Данная процедура позволяет определить отличительные особенности и полезность продуктов, предназначенных для медицины. Но выполняется она исключительно по желанию реализатора или изготовителя.

Добровольная сертификация не является альтернативой обязательной процедуре, а только ее дополнением. Порядок ее выполнения устанавливается в соответствии с системой ГОСТ Р. Выданные сертификаты могут использоваться исключительно на территории РФ, поскольку в странах-участницах ЕАЭС не предусмотрена сертификация на добровольной основе.
Такая возможность связана с наличием следующих положительных моментов:
- За счет наличия данного документа удается повысить узнаваемость компании для конечных потребителей;
- Улучшение конкурентоспособности в случае участия в конкурсах, торгах и тендерах;
- Расширение рынка сбыта, повышение привлекательности бренда для инвесторов;
- Приоритетные позиции при предоставлении льгот, грантов и другой финансовой помощи от государства;
- Подтверждение ориентации изготовителя на производство более безопасных, действенных и надежных продуктов.
Существуют определенные правила добровольной сертификации изделий медицинского назначения. На начальном этапе осуществляется подача заявки и запрашиваемых документов в выбранный Центр сертификации и регистрации медицинских изделий. К их числу относится:
- Технический паспорт на изготавливаемые продукты;
- Перечень изделий, которые должны пройти процедуру оценки соответствия;
- Данные о применяемой на производстве технике;
- Регистрационное удостоверение, уставные документы;
- Договор аренды производственных помещений.
Для предприятий-импортеров предусмотрен иной набор документов, в который входят:
- Полное название и реквизиты компании;
- Договора на поставку продукцию в РФ;
- Материалы технического характера, фотоснимки, руководство пользователя и др.
Кроме того, наличие данного документа позволяет изготовителю/реализатору воспользоваться знаком соответствия, который дает возможность сообщать потребителям о прохождении продуктом добровольной сертификации.
или позвоните нам
МСК: +7 499-350-48-69
СПб: +7 812-309-89-10
Сертификация медицинского оборудования в России
Для любой техники, используемой в медицинских целях в РФ, применяются правила регистрации и сертификации изделий медицинского назначения. В этот перечень включены устройства и приспособления, которые задействуют при реализации мероприятий диагностического, профилактического и лечебного характера в современных клиниках при уходе за пациентами и лицами с ограниченной двигательной активностью.
Требования стандартизации и сертификации медицинского оборудования применяются как к устройствам отечественного, так и иностранного производства.
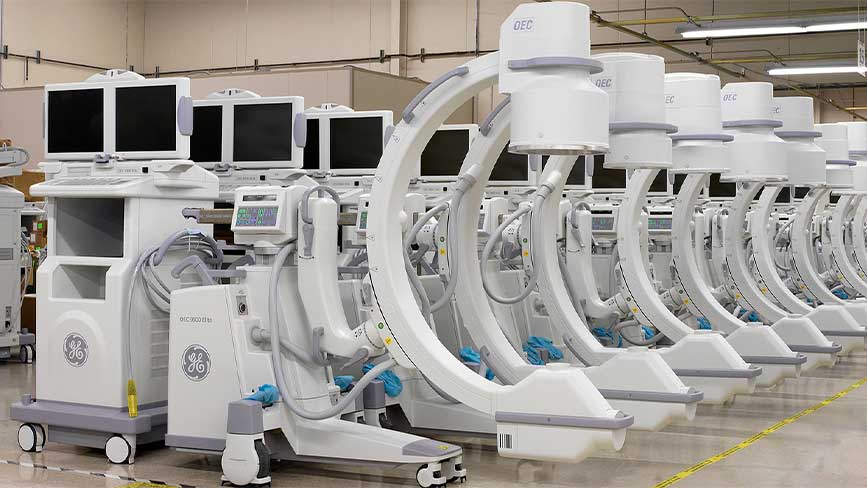
В список медтехники, которая подлежит сертификации на обязательных условиях, включены:
- Аппараты для функциональной диагностики;
- Устройства, применяемые в рамках эндоскопического, офтальмологического, увеличительного и радиодиагностического исследования;
- Приборы, используемые для целей рентгенографии;
- Инкубаторы для новорожденных;
- Электрорефлекторы;
- Приспособления, которые замещают функциональные характеристики отдельных системы и органов;
- Техника, используема для антисептических целей;
- Устройства, предназначенные для измерения давления;
- Приборы, устанавливаемые в палатах;
- Стерилизационное оборудование;
- Приборы для ЭКГ;
- Осветительная техника для медцентров и др.
Другие требования при сертификации медицинских изделий
Как известно, все продукты медицинского назначения способны оказывать воздействие на здоровье пациента. Именно поэтому для этой сферы предусмотрены дополнительные процедуры, позволяющие повысить их безопасность.
Обязательным условием, которое должно быть соблюдено при изготовлении и обращении техники оздоровительной специфики в Российской Федерации, считается прохождение регистрационной процедуры в уполномоченной структуре.
В случае, если регистрационная процедура в надзорном органе не была реализована, импорт подобной техники на территорию РФ является неправомерным.
Следует отметить, что получение регистрационного удостоверения является основным условием для оборота любого продукта медицинского назначения. Именно поэтому эта процедура выполняется до сертификации или декларации.
Что касается проведения испытаний токсикологического и технического характера, то они проводятся при участии аккредитованных лабораторных центров.
Реализация клинических исследований осуществляется в медцентрах, соответствующих требованиям Приказа Минздрава РФ от 16 мая 2013 г. N 300н.
Процедура сертификации или получение сертификата соответствия в 2022 году
Органы государственной власти занимаются разработкой дополнительных мероприятий по стабилизации и повышению устойчивости рынка товаров социального назначения, который подвергся внешним санкциям. В частности, было принято решение о введении упрощенной регистрационной процедуры.
Специалисты единого центра экспертизы и сертификации «ЕЦЭС КВОЛИТИ» помогут вам разобраться во всех тонкостях сертификации медицинских изделий, расскажут о всех принятых изменения и новых положениях в законе. Пройдите процедуру сертивикации при содействии специалистов с солидным профессиональным стажем, в укороченные сроки и с четким соблюдением действующих требований законодательства.
или позвоните нам
МСК: +7 499-350-48-69
СПб: +7 812-309-89-10

